このホームページを訪れて頂きありがとうございます。
ISO13485の品質マニュアルをお探しされているのでは?遠方の栃木県の企業様に購入して頂き大変お褒めを頂きました。ほかの会社の品質マンュアルを購入しましたが、ほとんど使えなく再度弊社の品質マニュアルを購入されました。でも弊社の品質マニュアルを購入される場合も悩まれたのでは、同じようにもし使えない品質マニュアルだったら。でも購入され安心されたそうです。それは使える品質マニュアルだったからです。
ISO 13485品質マニュアルとは
医療機器の品質マネジメントシステム(QMS)を運用・維持するために、組織全体の基本的な
品質のルール・仕組み・方針を体系的にまとめた文書です。
医療機器業界における「品質の設計図」
医療機器の設計、製造、販売、保守などに関わる企業が,規格(ISO 13485:2016)の要求事項に従い、自社の品質マネジメントシステム(QMS)を明確に定義し、
従業員・審査員・顧客・規制当局が理解・確認できるよう文書化したもの。
ISO13485品質マニュアルの必要性
- ISO13485とは
- 医療機器-品質マネジメントシステム-規制目的のための要求事項
-
JIS Q 13485:2018(ISO 13485:2016)
目次
0 序文 ········ 1
0.1 一般 ····· 1
0.2 概念の明確化 2
0.3 プロセスアプローチ ····· 3
0.4 JIS Q 9001 との関係······ 3
0.5 他のマネジメントシステムとの両立性 ··· 3
1 適用範囲 ·· 3
2 引用規格 ·· 4
3 用語及び定義 ··· 4
4 品質マネジメントシステム ······ 8
4.1 一般要求事項 8
4.2 文書化に関する要求事項 ······ 9
5 経営者の責任 ·· 11
5.1 経営者のコミットメント ····· 11
5.2 顧客重視 ····· 11
5.3 品質方針 ····· 11
5.4 計画 ···· 11
5.5 責任,権限及びコミュニケーション ····· 11
5.6 マネジメントレビュー · 12
6 資源の運用管理 ······ 13
6.1 資源の提供 ·· 13
6.2 人的資源 ····· 13
6.3 インフラストラクチャ · 13
6.4 作業環境及び汚染管理 · 13
7 製品実現 · 14
7.1 製品実現の計画 ··· 14
7.2 顧客関連のプロセス ···· 14
7.3 設計・開発 ·· 15
7.4 購買 ···· 17
7.5 製造及びサービスの提供 ····· 18
7.6 監視機器及び測定機器の管理 21
8 測定,分析及び改善 21
8.1 一般 ···· 21
8.2 監視及び測定 ······ 21
8.3 不適合製品の管理 23
8.4 データの分析 ······ 24
8.5 改善 ···· 24
附属書A(参考)JIS Q 13485:2005 とJIS Q 13485:2018 との内容の比較 ······ 26
附属書B(参考)JIS Q 13485:2018 とJIS Q 9001:2015 との関係 ··· 30
参考文献 ····· 36
解 説 · 38
この規格は,医療機器の設計・開発,製造,保管及び流通,据付け,附帯サービス,最終的な廃棄・処分,並びに関連する活動(例 技術支援)の設計・開発及び提供を含む医療機器のライフサイクルの一つ以上の段階に関係する組織が使うことができる品質マネジメントシステムの要求事項を規定する。
医療機器-品質マネジメントシステム-規制目的のための要求事項 JIS Q 13485:2018(ISO 13485:2016)の下記の4.2.2で品質マニュアルが規定されています。
4.2文書化に関する要求事項
4.2.1一般
品質マネジメントシステムの文書(4.2.4 参照)には,次を含める。
- 文書化した,品質方針及び品質目標の表明
- 品質マニュアル
- この規格が要求する文書化した手順及び記録
- プロセスの効果的な計画,運用及び管理を確実にするために必要であると組織が決めた記録を含む文書
- 適用される規制要求事項によって規定された他の文書
4.2.2 品質マニュアル
組織は,次を含む品質マニュアルを文書化する。
a) 品質マネジメントシステムの適用範囲。除外及び/又は不適用がある場合には,その詳細及びそれが正当であるとする理由
b) 品質マネジメントシステムについて文書化された手順又はそれらを参照できる情報
c) 品質マネジメントシステムのプロセス間の相互関係に関する記述
品質マニュアルには,品質マネジメントシステムで使用している文書体系の概要を記載する
4.2.4文書管理
品質マネジメントシステムで必要とする文書は管理する。ただし,記録は文書の一種ではあるが,4.2.5 に規定する要求事項に従って管理する。
文書化した手順は,次の活動に必要な管理を規定する。
- 発行前に,適切かどうかの観点から文書をレビューし,承認する。
- 文書をレビューする。また,必要に応じて更新し,再承認する。
- 文書の現在の改訂版の識別及び変更の識別を確実にする。
- 該当する文書の適切な版が,必要なときに,必要なところで使用可能な状態にあることを確実にする。
- 文書が読みやすく,容易に識別可能な状態であることを確実にする。
- 外部で作成され,組織が品質マネジメントシステムの計画及び運営に必要と判断した文書を明確にし, その配付の管理を確実にする。
- 文書の劣化又は紛失を防ぐ。
- 廃止文書が誤って使用されないようにする。また,廃止文書に適切な識別をする。
組織は,その決定の基礎となる関連する背景情報を入手できる立場にある,最初に承認した部署又はそ の他の指名した部署が,文書の変更をレビューし,承認することを確実にする。
組織は,廃止した管理文書の少なくとも一部を保管しておく期間を定める。この期間は,その医療機器の製造及び検査に使用した文書が,少なくとも組織が定めたその医療機器の寿命の期間は入手できること を確実にする。ただし,この期間は,結果として得られる全ての記録(4.2.5 参照)の保管期間又は適用される規制要求事項によって定められた期間より短くしない。
 ISO13485品質マニュアルの作成で苦労しました。
ISO13485品質マニュアルの作成で苦労しました。
-
規格要求の言い回しが抽象的・難解で、自社の実務にどう落とし込むか悩む
-
QMSの適用範囲(4.2.2)や除外の根拠が説明しづらい
-
各業務プロセス(設計、製造、検査、保守など)の関連性が複雑で整理が難しい
-
プロセスマップや業務フローの作成が大変
-
製品のライフサイクルに合わせた「有効性の維持方法」がうまく書けない
-
「ソフトウェアバリデーション」などの実施記録とルールの記載が面倒
-
製造・滅菌・包装工程などバリデーションが必要な箇所の明示が漏れやすい
-
リスクマネジメント(ISO 14971との整合)がQMSにどう紐づくか不明確になりがち
-
文書管理台帳・記録一覧・保存期間などを明記するのが手間
-
「誰が承認・配布・管理しているか」など権限設計の明文化が難しい
-
品質記録の電子システムを使っている場合、管理手順との整合が複雑
-
設計プロセスの文書化(7.3項)が他業界より細かく要求される
-
設計変更の記録、再バリデーションの要否などの基準設定が曖昧になりやすい
-
苦情処理プロセスと「是正処置」との違いの明確化が難しい
-
市販後監視とのつながりを表現しづらい
-
フィードバック情報の収集方法・評価基準など、運用と文書が乖離しがち
-
医療機器は専門性が高く、教育内容・力量基準を詳細に記載する必要がある
-
職種別にどの教育が必須かを明記するのが手間
-
外注業者や派遣スタッフの教育管理の範囲設定が曖昧になりがち
ISO13485品質マニュアルのサンプルを活用のメリット
- 担当者が悩まなくて良いです。
- 時間の節約と人件費の節約(お金の節約)
- 作成期間の短縮
- 早く完成できます
- 内部監査、マネジメントレビューに早く取り掛かれる
- 審査,認定時期がはやまります。
- 安心の品質マニュアル
- いろいろなISO13485品質マニュアルを購入しても、審査を受けるには、多く不安を抱く品質マニュアル。やはり、審査に合格するほどのレベルの充実した品質マニュアルを期待購入される方が大部分。
- 自社用に簡単に作成
- マイクロソフト社のWordで作成されているISO13485品質マニュアルなので、自社用に簡単に作成できる内容のしっかりした品質マニュアルを作成することができる
- 要求事項を網羅
- ISO13485要求事項を漏らさず作成されている
- 参照文書が明記
- 下位文書への参照文書が分かりやすい
- 一目で分かる全体文書
- マネジメントシステムに必要な文書化した情報がすぐわかる。
- 必要な記録が分かる
- マネジメントシステムに必要な運用記録様式もどんなものが必要かすぐわかる。
- 審査機関の要求事項を理解していないと、ISO13485品質マニュアルの作成には、苦労するが、ISO13485要求事項と品質マニュアルを対比していくと分かりやすい。
デミリット
- 完成が遅れ、運用に進まない
- 計画していた完成時期を大幅に超え、完成が大幅に遅れる
- 認定審査において、品質マニュアルの理解周知が試されますが、品質マニュアルが読まれていない
- 予め計画していた取得時期の審査機関の審査が延びてしまう
- 多くの関係者か品質マニュアルの作成に関与していない場合に起こりえます
ISO13485品質マニュアルの案内
ISO13485品質マニュアルの完成が早くできればできるほど、登録審査を早く受けられ早く認定登録できる。
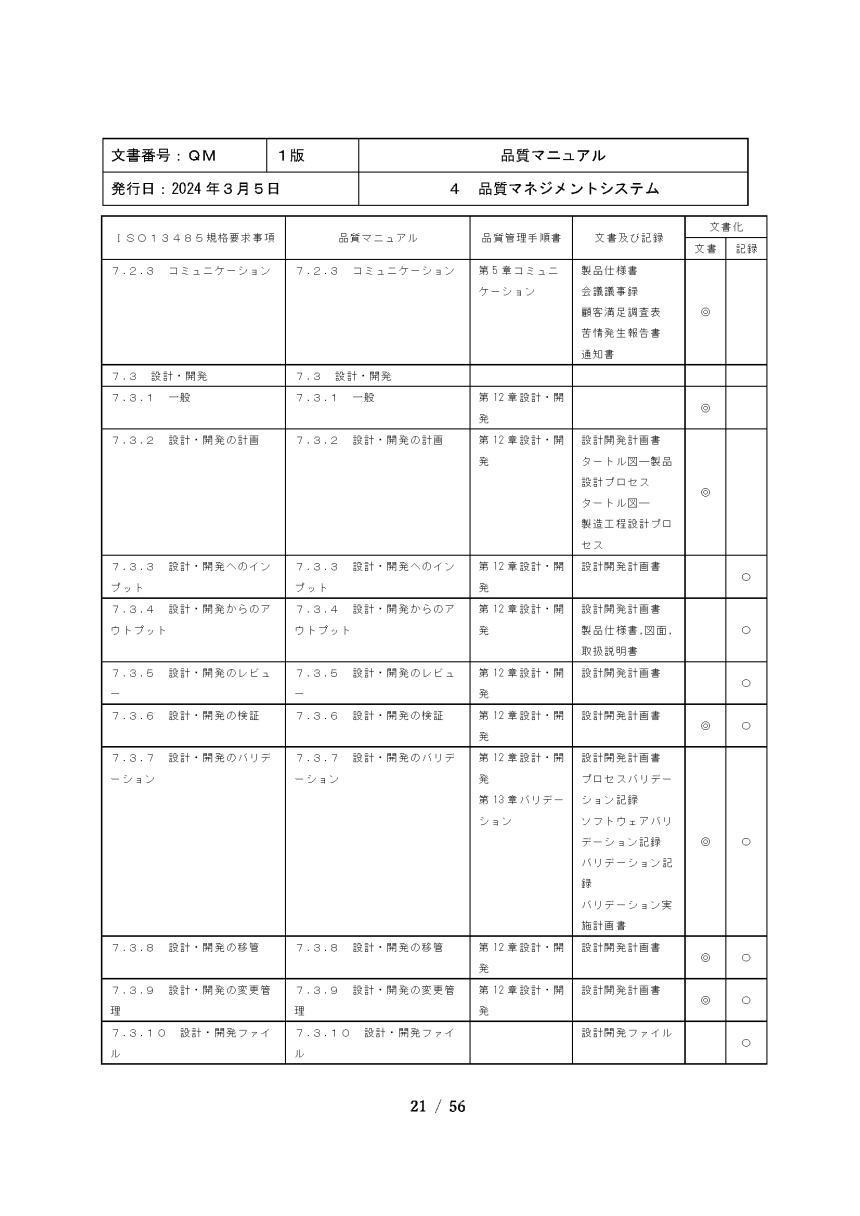
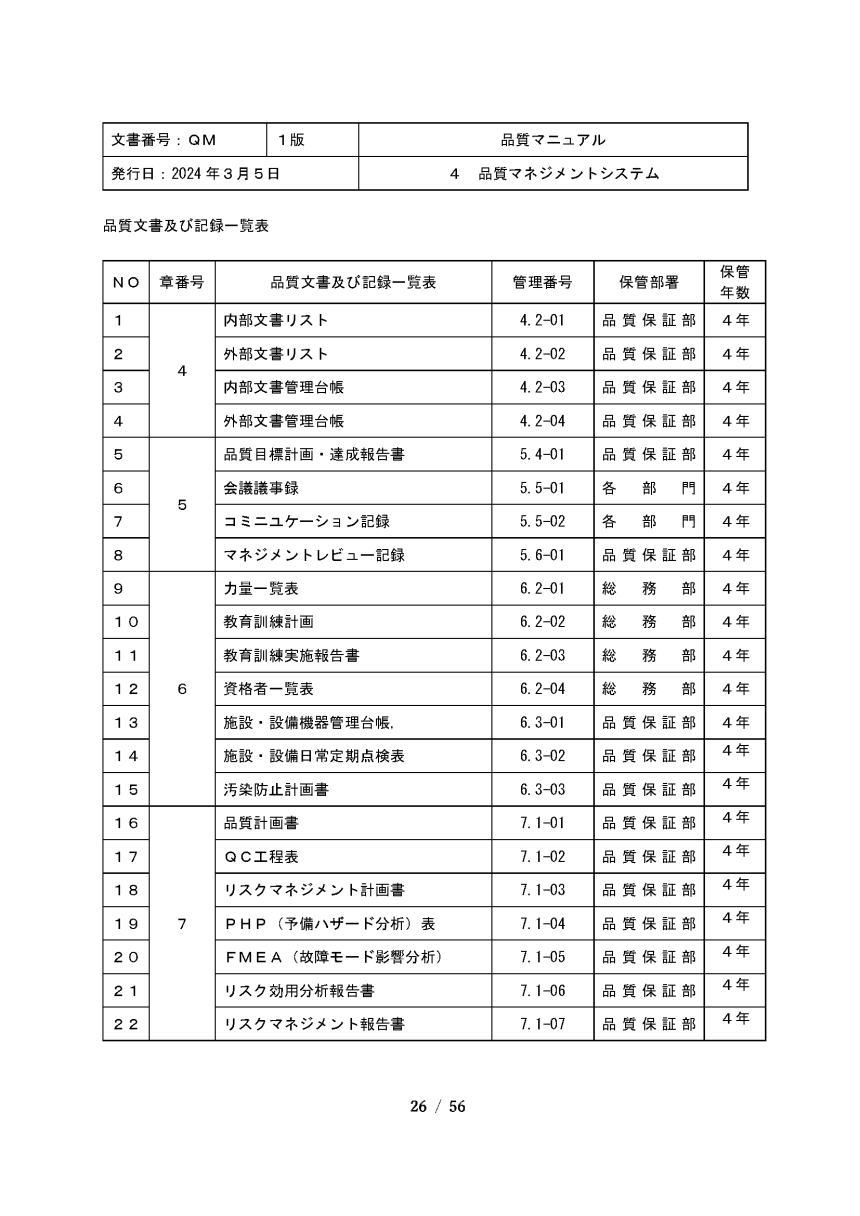
A4版で製本されています
USBに品質マニュアル WORD版が収録
全56ページからなっています。



-
サポートのご案内
-
もうすぐ終了!今だけの無料特典 (令和7年6月30日まで)
弊社のISO13485品質マニュアル等の下記の文書の4つの文書①ISO13485品質マニュアル
➁ISO13485品質管理規定
➂ISO13485記録
④ISO13485内部監査チェックリスト
を購入された方限定で下記の無理サービスを提供します。
期間は、令和7年6月30日までの限定無料サービスです。
(1)品質マニュアルのカスタマイズ指導で安心
※ISO13485取得の取り組みについての不明な点もお聞きすることが
できます
お客様の適用範囲の特性に応じたカスタマイズ -実務に即した具体的
なカスタマイズ
方法 1回訪問させて頂き指導致します
購入後に日時の打合せさせて頂きます。
時間;10時から16時
指導方法;訪問指導
参加要員;各部署の責任者
無料;指導料、航空券、交通費宿泊費全額無料
ただし、最寄り駅までは送迎 をお願いします。
-
- お問い合わせは下記フォームより